薬の分布(薬物動態)
吸収された薬は全身循環系に入り、体液によって全身に分布します。
しかし、すべての組織や体液に分布するのではありません。
薬の特性や患者の状態によって、分布状況や薬効も違いがでてきます。
スポンサーリンク
脂溶性の高い薬物
脂溶性の高い薬物は脂肪組織に分布します。
代表例として,全身麻酔薬のチオペンタール(医薬品例:ラボナール注射用)、セコバルビタール(医薬品例:注射用アイオナール・ナトリウム)や睡眠薬があります。
脳は脂質が多いため、これらの薬は脳に分布しやすいです。
血液脳関門(blood-brain-barrier)
血液脳関門は、脳に入る物質を選別する役割を担っています。
上記のように脂溶性の高い薬は脳に分布しやすいのですが、脂溶性でない薬やイオン化している薬は移行しません。血液脳関門が侵入を阻止するからです。
血漿タンパクとの結合性
血漿タンパクに結合しやすい薬は、主に血管内に分布します。
また、イオン化しやすい薬は、主に細胞外液に分布します。
特定の器官に親和性の高いもの
薬には特定の器官に親和性が高く、その器官に選択的に分布するものがあります。
例えば、重金属は骨組織に蓄積します。
また、ヨウ素は能動輸送により甲状腺に取り込まれます。
血漿タンパクと薬の結合率
薬の分布を考える上で重要になるのは、血漿タンパクと薬の結合率です。
多くの薬は吸収された後血漿タンパクと結合するのですが、100%結合するわけではありません。
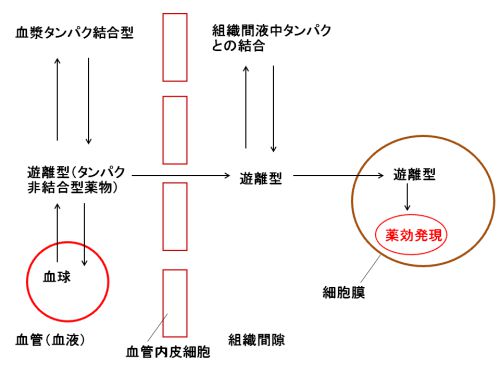
血漿タンパクと結合している結合型と、結合していない遊離型が共存しています。
これらは、くっついたり離れたりを繰り返しながら、結合型と遊離型の両方を一定の割合で保っています。
薬が作用を現すのは遊離型です。
なぜなら、血漿タンパクと結合した薬は毛細血管壁を透過することが困難であるからです。
血漿タンパクとの結合率が高い薬の場合、結合率が変化することで薬効が強く現れてしまうことがあり注意が必要です。
血液中の薬は、一部は血球内に取り込まれますが、血漿中では血漿タンパク(主にアルブミン)と結合しています。
そのため腎疾患などによってアルブミンの血中濃度が減少したり、他のタンパク結合率の高い薬と併用することで結合できるタンパク質が少なくなり、遊離型が増えてしまいます。
薬効を現す遊離型が増えるということは、それだけ薬効が強く現れる危険性が高まるということです。
例えば、血漿タンパク結合率の高い薬としてワルファリン(医薬品名:ワーファリン)があります。
ワルファリンの結合型が98%で遊離型が2%とします。薬効を現しているのは遊離型の2%です。
しかし、なんらかの作用により結合型が96%に減少し、遊離型が4%に増加したとします。そうなると、遊離型は2%から4%の2倍に増え、理論上は薬効も2倍になると考えられるのです。
抗菌薬と臓器移行性
抗菌薬を選択する時も、「薬がどの臓器に分布しやすいか」という臓器移行性を考慮しなければなりません。
原因菌に感受性のある抗菌薬を投与したとしても、薬が感染源である臓器に移行しなくては意味がありません。
ただし敗血症の場合は臓器移行性を考慮する必要はありません。
臓器移行性の高い抗菌薬の例
胆道感染症
「ペニシリン系」
- ドイル(アスポキシシリン水和物)
- ペントシリン(ピペラシリンナトリウム)etc
「セフェム系」
- セファメジン(セファゾリンナトリウム)
- メイセリン(セフミノクスナトリウム水和物)
- パンスポリン(セフォチアム塩酸塩)
- モダシン(セフタジジム水和物)
- ロセフィン(セフトリアキソンナトリウム水和物)etc
市中肺炎
「ニューキノロン系」
- クラビッド(レボフロキサシン水和物)
- タリビット(オフロキサシン)
- ジェニナック(メシル酸ガレノキサシン水和物)
「セフェム系」
- メイアクトMS(セフジトレンピボキシル)
- フロモックス(セフカペンピボキシル)etc
尿路感染症
- 「腎排泄型のペニシリン系」
- 「セフェム系」
- 「ニューキノロン系」etc
髄膜炎(中枢神経系へ移行性の高い抗菌薬)
「セフェム系」
- セフォタックス(セフォタキシムナトリウム)
- ロセフィン(セフトリアキソンナトリウム)
- モダシン(セフタジジム水和物)
- シオマリン(ラタモキセフナトリウム)etc
胎盤・母乳への移行性
妊婦の服薬可否
胎盤への薬の移行は、一般に単純拡散と考えられています。
つまり、分子型で脂溶性の高い薬が胎盤へ移行しやすいと言えます。
また、胎盤は毒物も簡単に通過して胎児に移行するため注意が必要です。
妊婦や授乳婦への薬の影響はたびたび医療者を悩ませる問題です。
添付文書を読んでも、はっきりとしたデータを提示している薬は少ないです。それは、医薬品の臨床試験では、倫理的な問題から妊婦・授乳婦は一般的に除外対象となっているからです。
よって、「少しでもリスクのある薬はやめておこう」ということになってしまいます。
薬による催奇形性が最も問題になる時期は、妊娠4週〜7週末です。サリドマイドによる胎児奇形が起こったのもこの時期です。
こういった歴史的な薬害事件もあり、妊婦・授乳婦への投薬に躊躇していまうのは仕方ありません。
しかし、リスクを心配するあまり薬物治療をしないことは、患者に不利益をもたらします。
どうしても薬物治療が必要な時は、少しでも危険性の低い薬を選択する必要があります。
日本では妊婦・授乳婦に対する薬のリスク分類が整備されてないことから、海外の公的リスクカテゴリーや成書を参考にすることがあります。
有名なものとして
- 米国医薬品食品局(FDA)のPregnancy Category(FDA-PC)
- オーストラリア保健省・薬品・医薬品行政局(TGA)処方薬諮問(シモン)委員会の分類基準(ACPM-PC)
があります。
成書としては
- 「妊娠・授乳女性の薬ハンドブック 第3版 」(メディカル・サイエンス・インターナショナル)
- 「授乳婦と薬―薬剤の母乳移行性情報とその評価」(じほう)
- 「薬剤の母乳への移行」(南山堂)
などがあります。
また、参考になるホームページとしては
があります。
授乳婦の服薬可否
日本の医療においては、授乳婦への投薬と服薬中の授乳の可否については、医療用医薬品添付文書の使用上の注意「8. 妊婦、産婦、授乳婦への投与」の項の記載に従うのが原則とされています。
しかし、多くの添付文書は「母乳中へ移行することが報告されているので、投与中は授乳を避けさせること」と記載されていることが多く、服薬中の授乳の可否が判断できるものではありません。それでリスクを怖れて服薬しないことが多いのですが、どうしても服薬したいケースもあります。
母乳は新生児にとって最良の栄養源であり、免疫グロブリン、ラクトフェリンなど免疫力を高める物質も入っています。母親と子供も絆を強める意味でも授乳の重要性は高く、「服薬しなければいけないから授乳はやめておこう」となかなか割り切れるものでもありません。
ただ、ほとんどの薬は母乳に移行すると言われていますが、実際その量は非常にすくないです。薬を飲んでいるから母乳をあげることを必ず諦めなければならないものでもないのです。
以下のホームページには「授乳中に安全に使用できると思われる薬」と「授乳中の治療に適さない薬」の一覧が掲載されています。
ただし、絶対に授乳婦に投与してはいけないものはあります。
下図は、授乳中の母親には投与が禁忌とされている薬です。
| 一般名 | 商品名 | 乳児に現れる症状、微候あるいは乳汁分泌への影響 |
|---|---|---|
| ブロモクリプチン | パーロデル | 乳汁分泌抑制 |
| コカイン | 塩酸コカイン | コカイン中毒 |
| シクロフォスファミド | エンドキサン | 免疫抑制の可能性、好中球減少 |
| シクロスポリン | サンディミュン/ネオーラル | 免疫抑制の可能性 |
| ドキソルビシン | アドリアシン | 免疫抑制の可能性 |
| エルゴタミン | ジヒデルゴット | 免疫抑制の可能性 |
| リチウム | リーマス | 乳児の血中濃度が治療濃度の1/3〜1/2になる |
| メトトレキサート | リウマトレックス | 免疫抑制の可能性、好中球減少 |
授乳婦と薬―薬剤の母乳移行性情報とその評価 p18
また、海外のデータを参考にすることもあります。
WHOなどの公的機関やMedications and Mothers' Milk(Hale)の編纂した授乳と薬物の専門書において、服薬中も適合(Compatible)、おそらく適合(Probably Compatible)と判断されている薬もあります。

